Opracowano na podstawie: Minimally invasive surgical treatments for benign prostatic hyperplasia
V. Tzortzis, S. Gravas, J.JM.C.H. de la Rosette
Eur Urol Suppl 2009; 8: 513-522
Pod pojęciem minimalnie inwazyjnej metody leczenia (minimally
invasive surgical treatment - MIST) kryje się każdy zabieg mniej
inwazyjny niż leczenie operacyjne wykonany dla osiągnięcia tego
samego celu. Obecnie za referencyjny standard MIST w przypadku
łagodnego rozrostu stercza (benign prostatic hyperplasia - BPH)
uważana jest przezcewkowa elektroresekcja gruczołu krokowego
(transurethral resection of the prostate - TURP). Wiąże się ona jednak
z 10% ryzykiem takich powikłań, jak:
- krwawienie;
- zespół poresekcyjny (spowodowany przedostawaniem się znacznych ilości płynu irygacyjnego do naczyń krwionośnych;
skutkiem tego mogą być: hiperwolemia, hiponatremia, nudności, wymioty, bóle głowy, niepokój, drażliwość, nadciśnienie tętnicze, drgawki, obrzęk płuc, niewydolność nerek);
- zwężenie cewki moczowej;
- zwężenie szyi pęcherza moczowego;
- zaburzenia funkcji seksualnych.
Co więcej, 10-15% chorych wymaga kolejnej operacji w ciągu następnych 10 lat, śmiertelność zaś wynosi 0,2-2,5%.
W leczeniu BPH zostały najlepiej przebadane i zaakceptowane następujące techniki MIST:
- Przezcewkowa termoterapia mikrofalowa (transurethral microwave thermotherapy - TUMT)
- Przezcewkowa ablacja igłowa (transurethral needle ablation - TUNA)
- Zabiegi laserowe, w tym enukleacja stercza laserem holmowym
(holmium laser enucleation of the prostate - HoLEP)
oraz waporyzacja laserem potasowo-tytanowo-fosforanowym
(potassium titanyl phosphate - KTP).
Przezcewkowa termoterapia mikrofalowa - TUMT
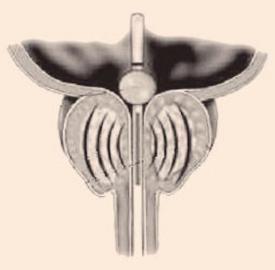
W TUMT używa się specjalnego cewnika z anteną (ryc. 1). Emituje ona mikrofale, które powodują wzrost temperatury tkanki stercza. Przekroczenie temperatury 45°C powoduje efekt cytotoksyczny (martwica koagulacyjna).
Inne postulowane mechanizmy działania TUMT to:
- zniszczenie unerwienia α-adrenergicznego powodujące spadek napięcia mięśni gładkich cewki sterczowej;
- apoptoza.
Urządzenia wykorzystują częstotliwości fal 915 MHz i 1296 MHz.
Różnią się między sobą budową anteny, systemem chłodzenia, czasem
terapii i sposobem monitorowania procesu. Konstrukcja anteny
zdaje się mieć większy wpływ na efekt zabiegu niż częstotliwość fal.
Najpowszechniej stosowane urządzenia do TUMT to: Prostatron
(Urologix, Minneapolis, MN, USA); Targis (Urologix); CoreTherm
(ProstaLund, Lund, Sweden) oraz TMx - 2000 (TherMatrx Inc,
Northbrook, IL, USA).
|
Specjalny cewnik z anteną |
 |
Skuteczność i bezpieczeństwo
Wyniki zbiorczej analizy dostępnych badań porównujących TUMT z TURP:
- redukcja nasilenia objawów w skali punktowej po 12 miesiącach od zabiegu: 65% dla TUMT i 77% dla TURP;
- wzrost tempa przepływu cewkowego o 70% dla TUMT i 119% dla TURP;
- w jednym z badań stwierdzono przewagę CoreTherm nad innymi urządzeniami w zakresie parametrów subiektywnych i obiektywnych; inne badania nie wykazały przewagi żadnego z urządzeń.
Wyniki porównania TUMT z terapią farmakologiczną:
- potwierdzono przewagę TUMT w zakresie poprawy przepływu cewkowego i redukcji nasilenia objawów po 6 i 18 miesiącach w porównaniu z terazosyną.
Zabieg jest dobrze tolerowany. Większość pacjentów zgłasza dyskomfort w okolicy krocza i parcia naglące. Leki przeciwbólowe są podawane przed zabiegiem lub podczas zabiegu. Wyniki badań wskazują, że główną zaletą TUMT jest niższy niż dla TURP odsetek powikłań.
Działania niepożądane związane z TUMT:
- przedłużony okres utrzymywania cewnika;
- dyzuria;
- parcia naglące;
- zatrzymanie moczu.
Ryzyko zwężenia cewki lub szyi pęcherza wymagające zabiegu jest
mniejsze po TUMT niż po TURP.
Rzadziej występuje wytrysk wsteczny (współczynnik ryzyka w porównaniu z TURP: 0,39) i zaburzenia wzwodu.
Trwałość efektu
U chorych poddanych TUMT istnieje większe prawdopodobieństwo konieczności ponownego leczenia z powodu niepowodzenia
leczenia pierwotnego (7,54 na 100 osobolat) w porównaniu z TURP
(1,05 na 100 osobolat).
Przezcewkowa ablacja igłowa - TUNA
Aparat do przeprowadzania TUNA emituje fale elektromagnetyczne o częstotliwości radiowej (460 kHz), które powodują miejscowy
wzrost temperatury powyżej 100°C, powodując martwicę tkanki gruczolaka stercza. Na końcu cewnika znajdują się dwie elastyczne
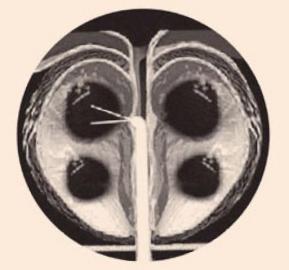
igły, które są rozmieszczone pod kątem 40° w stosunku do siebie i pod kątem 90° do cewnika (ryc. 2). Cewka moczowa jest chroniona przed działaniem wysokiej temperatury za pomocą teflonowych
osłon.
|
Dwie elastyczne igły na końcu cewnika, rozmieszczone pod kątem 40°
w stosunku do siebie i pod kątem 90° do cewnika |
 |
Skuteczność i bezpieczeństwo
W metaanalizie Boyle i wsp. przeanalizowali wyniki 2 randomizowanych badań, 2 nierandomizowanych protokołów i 10 badań pozbawionych grup kontrolnych.
Stwierdzono, że zastosowanie TUNA powoduje:
- zmniejszenie nasilenia objawów o 50%;
- wzrost maksymalnego tempa przepływu cewkowego (Qmax) o 57-70% (dla TURP poprawa wyniosła 148%);
- zmniejszenie ciśnienia wypieracza w czasie mikcji, chociaż u znacznej liczby chorych po zabiegu nadal wykazano istnienie przeszkody podpęcherzowej;
- nie zaobserwowano istotnej redukcji objętości stercza;
- w porównaniu z TURP zanotowano statystycznie istotne różnice na korzyść resekcji przezcewkowej.
Omawiane parametry oceniano rok po zabiegu. Efekt zabiegu utrzymywał się po 5 latach, choć z czasem słabł.
TUNA jest na ogół przeprowadzana ambulatoryjnie, w znieczuleniu miejscowym, jednak niektórzy chorzy wymagają dożylnej sedacji.
Doskonały profil bezpieczeństwa został dowiedziony w wielu krótko i długoterminowych badaniach.
Najczęściej występujące działania niepożądane to:
- przejściowy krwiomocz, niewymagający leczenia;
- zatrzymanie moczu, ustępujące zwykle po 12-48 godz.;
- po tygodniu 90-95% chorych oddaje mocz samodzielnie;
- objawy podrażnieniowe.
Rzadko (<4%) występuje zakażenie układu moczowego lub zapalenie
najądrza.
Zwężenia cewki stwierdzano w 0-1,5% przypadków.
Zabieg nie ma wpływu na trzymanie moczu.
W mniejszym niż TURP stopniu wpływa na wzwody i wytrysk.
Łącznie stwierdzono o 19% mniej powikłań po TUNA niż po TURP
Trwałość efektu
Poprawa subiektywnych i obiektywnych parametrów uzyskana
w wyniku zastosowania TUNA utrzymuje się co najmniej 5 lat.
Dłuższych badań nie prowadzono. Efekt TURP był w każdym
punkcie obserwacji lepszy niż efekt TUNA.
19% pacjentów po zastosowaniu TUNA wymaga wykonania następnego zabiegu z powodu niepowodzenia. Odsetek ten jest 7 razy większy niż dla TURP.
Dobór chorych
Zaobserwowano, że chorzy z gruczołem krokowym o objętości
>75 ml lub z izolowaną przeszkodą na poziomie szyi pęcherza bądź
z powiększeniem środkowego płata gruczołu nie są idealnymi kandydatami do leczenia TUNA. Inne badania wykazały jednak,
że wielkość gruczołu krokowego i jego kształt nie wpływały na odpowiedź na leczenie. TUNA nie jest zalecana u chorych z metalowymi protezami miednicy lub rozrusznikiem serca.
Zabiegi z użyciem lasera
Technologia laserowa została zastosowana po raz pierwszy w leczeniu przeszkody podpęcherzowej spowodowanej przez BPH ponad
15 lat temu. W zależności od długości fali, mocy i rodzaju emisji lasera (ciągła albo impulsowa) używa się różnych technik usuwania
tkanki gruczolaka: koagulacji, waporyzacji, resekcji lub preparowania.
W leczeniu BPH stosowano cztery typy lasera:
- laser neodymowo-yagowy (Nd:YAG); YAG (yttrium aluminium garnet) - granat itrowo-glinowy
- laser holmowy (Ho: YAG)
- laser potasowo-tytanowo-fosforanowy (KTP: YAG)
- laser diodowy.
Opisano następujące zabiegi wykonywane za pomocą lasera:
- laserowa przezcewkowa ablacja gruczołu krokowego (visual laser ablation of the prostate - VLAP)
- laserowa koagulacja śródmiąższowa gruczołu krokowego (interstitial laser coagulation - ILC)
- fotoselektywna waporyzacja gruczołu krokowego (photoselective vaporisation of the prostate - PVP)
- nacięcie szyi pęcherza laserem holmowym (holmium laser bladder neck incision - HoBNI)
- ablacja gruczołu krokowego laserem holmowym (holmium laser ablation of prostate - HoLAP)
- resekcja gruczołu krokowego laserem holmowym (holmium laser resection of prostate - HoLRP)
- enukleacja gruczołu krokowego laserem holmowym (holmium laser enucleation of prostate - HoLEP).
Obecnie tylko dwie procedury mogą podważyć pozycję TURP jako
standardu leczenia chirurgicznego: HoLEP oraz waporyzacja stercza za pomocą lasera KTP o dużej mocy.
Laserowa enukleacja gruczołu krokowego (HoLEP)
Laser holmowy jest laserem impulsowym o fali długości 2140 nm,
która jest silnie pochłaniana przez wodę. Głębokość penetracji
tkanki gruczołu krokowego wynosi tylko 0,4 mm. Osiągana gęstość
energii jest wystarczająca, aby ogrzać tkankę gruczołu krokowego
do temperatury >100°C, co powoduje waporyzację bez powstawania
głębokiej koagulacyjnej martwicy tkanek. Gilling i wsp. byli pionierami tych technik. Zabieg wykonuje się w warunkach ciągłego
przepływu płynu, przy użyciu specjalnego resektoskopu i włókna
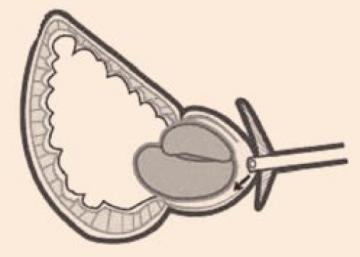
emitującego na wprost światło o wysokiej energii (60-80 W). Procedurę zaczyna się od nacięcia szyi pęcherza na godz. 5 i 7. Prowadząc
cięcie w płaszczyźnie między gruczolakiem a torebką stercza, uwalnia się płaty środkowy i boczne. Fragmenty gruczolaka należy przemieścić do pęcherza i usunąć przy użyciu morcelatora (ryc. 3).
|
|
 |
Początkowo HoLEP został zaproponowany jako alternatywa
dla TURP w leczeniu gruczolaków małej i średniej wielkości. Po opublikowaniu wyników badań przeprowadzonych przez Kuntza i Lehricha, w których dokonano porównania HoLEP z otwartą adenomektomią (open prostatectomy - OP), przeprowadzono więcej badań,
które potwierdziły bezpieczeństwo i skuteczność tej terapii, również
u chorych z gruczołem krokowym znacznych rozmiarów. Z tych
powodów HoLEP został zdefiniowany jako endourologiczna alternatywa dla OP.
Skuteczność i bezpieczeństwo
- HoLEP vs TURP
W pierwszej metaanalizie badań porównujących HoLEP i TURP
stwierdzono przewagę HoLEP w zakresie zmniejszenia przeszkody
podpęcherzowej dla gruczolaków większych niż 50 g. Kolejna metaanaliza nie wykazała różnic między tymi dwiema metodami leczenia
w zakresie poprawy wartości Qmax po 12 miesiącach oraz wystąpienia powikłań, takich jak zwężenie cewki, toczenie krwi, konieczność
ponownego zabiegu. Natomiast łączna liczba powikłań była istotnie mniejsza w przypadku HoLEP (8%) niż TURP (16%).
Zbiorcza analiza wykazała przewagę HoLEP w zakresie: czasu cewnikowania, czasu hospitalizacji oraz utraty krwi.
- HoLEP vs OP
Badania wykazały, że dla gruczolaków >70 g obiema metodami uzyskuje się podobne wyniki czynnościowe oceniane po 2 latach. Nie ma
również różnic w odsetku reoperacji. Czas utrzymywania cewnika,
czas hospitalizacji i utrata krwi były mniejsze po zabiegu HoLEP.
Trwałość efektu
Subiektywna i obiektywna poprawa po HoLEP utrzymuje się co najmniej 6 lat, a odsetek reoperacji spowodowany odrostem gruczolaka
wynosi 4,2%. Główną przeszkodą dla upowszechnienia tej metody jest długa krzywa uczenia, wynosząca 30-50 przypadków.
Waporyzacja stercza z użyciem lasera KTP
Światło lasera neodymowo-yagowego o długości fali 1064 nm przenikając przez kryształ KTP (ryc. 4) dwukrotnie zwiększa częstotliwość i skraca długość fali, stając się widzialne w widmie koloru
zielonego (green-light laser - laser zielony). Zielone światło jest selektywnie pochłaniane przez hemoglobinę, która działa jak wewnątrzkomórkowy chromofor. Absorpcja prowadzi do natychmiastowego usunięcia tkanki gruczołu poprzez szybką fototermiczną
waporyzację podgrzanej wewnątrzkomórkowej wody (stąd nazwa fotoselektywna waporyzacja stercza - PVP). Dzięki małej głębokości penetracji lasera do tkanki (0,8 mm) powstająca strefa martwicy
jest ograniczona (1-2 mm), co przyczynia się do lepszej wydajności i selektywności waporyzacji oraz do powstania loży podobnej
jak po TURP.
Pierwsze zabiegi przeprowadzano przy użyciu urządzenia o mocy
60 W. Jednak ze względu na długi czas zabiegu szybko skonstruowano laser zielony o mocy 80 W. Pierwsze wyniki uzyskane przy
użyciu nowego urządzenia opublikowano w 2003 roku.
|
|
 |
Skuteczność i bezpieczeństwo lasera KTP 80 W
- Laser KTP vs TURP
Dotychczas przeprowadzono tylko dwa badania z randomizacją porównujące użycie lasera KTP i TURP. Bouchier i wsp. wykazali, że
KTP przewyższa TURP jeśli chodzi o czas cewnikowania, utratę
krwi i czas hospitalizacji. Po 6 miesiącach w obu grupach uzyskano
podobną redukcję nasilenia objawów, natomiast większą redukcję
objętości stercza po TURP. Odsetek wczesnych reoperacji był
mniejszy po TURP.
Horasansli i wsp. porównali krótkoterminowe wyniki PVP i TURP
u chorych z gruczołami krokowymi o objętości >70 ml:
- czas operacji był znamiennie dłuższy w przypadku KTP;
- czas utrzymywania cewnika i czas hospitalizacji był dłuższy po TURP;
- trzech pacjentów z grupy TURP wymagało transfuzji krwi;
- po 6 miesiącach stwierdzono znamienną statystycznie różnicę w IPSS, Qmax i PVR na korzyść TURP;
- zachowanie funkcji seksualnych i występowanie wytrysku wstecznego były podobne w obu grupach;
- redukcja objętości stercza była większa po TURP (62,9% vs 40,5%);
- siedmiu chorych (17,9%) w grupie poddanej PVP wymagało reoperacji z powodu nieustępującej przeszkody podpęcherzowej;
po TURP żaden chory nie wymagał wczesnej reinterwencji;
- trzech chorych (8,1%) w grupie TURP i dwóch chorych (5,1%) w grupie PVP przeszło uretrotomię wewnętrzną z powodu
zwężenia cewki moczowej rozpoznanego w okresie obserwacji.
- Laser KTP vs otwarta adenomektomia
W jedynym badaniu dotyczącym chorych z gruczolakiem >80 ml
autorzy stwierdzili:
- dłuższy czas PVP niż operacji;
- krótszy czas utrzymywania cewnika i hospitalizacji;
- częstszą konieczność toczenia krwi po operacji otwartej;
- lepsze wyniki IPSS QOL po adenomektomii;
- brak różnicy w zakresie wartości Qmax, PVR i wyników ankiety
IIEF-5 (5 item International Index of Erectile Function);
- podobną, małą liczbę powikłań, tj. zwężenie cewki moczowej,
zwężenie szyi pęcherza, utrzymująca się przeszkoda
podpęcherzowa wymagająca ponownego zabiegu.
Trwałość efektów
W 3-letniej obserwacji stwierdzono trwałą poprawę w zakresie parametrów czynnościowych i odsetek reinterwencji wynoszący 4,3%.
W grupie 500 mężczyzn z zatrzymaniem moczu, stosujących antykoagulanty lub w zaawansowanym wieku, o średniej objętości stercza 56 ml nie stwierdzono ciężkich powikłań śródoperacyjnych,
czas zabiegu wyniósł średnio 66 min, czas utrzymywania cewnika
1,8 dnia, czas hospitalizacji po zabiegu 3,7 dnia. Wszystkie parametry
czynnościowe poprawiły się, a odsetek reinterwencji wyniósł 6,8%.
Laser KTP 120 W
Pomimo udowodnionej skuteczności 80-watowego lasera KTP, waporyzacja dużych gruczolaków jest nadal czasochłonna. Dlatego
opracowano laser o jeszcze większej mocy: GreenLight High Performance System (HPS). Ten diodowy laser emitujący fale o długości
532 nm dostarcza energię o mocy 120 W, co skutkuje zwiększeniem
skuteczności waporyzacji. Jedna z różnic między tym systemem
i 80-watowym laserem KTP polega na tym, że ognisko maksymalnej
mocy ma tu długość nawet 3-5 mm, co pozwala na skuteczniejszą
waporyzację niezależnie od zmian odległości między włóknem
a tkanką. Ta nowa technika niesie ze sobą ryzyko perforacji pęcherza
moczowego, uszkodzenia ujść moczowodów czy perforacji torebki
stercza i otwarcia dużych zatok żylnych. Zwiększona waporyzacja
może również wpłynąć na pogorszenie jakości obrazu wskutek powstawania większej ilości pęcherzyków gazu i skutkować mniej skuteczną hemostazą oraz przyspieszoną degradacją włókien lasera.
Posługiwanie się laserem KTP HPS wymaga dłuższej krzywej uczenia.
W grupie pacjentów ze średnią objętością stercza 61 ml średnie czasy użycia lasera i zabiegu wyniosły odpowiednio 13 min i 30 min.
Wszystkie zabiegi wykonano w warunkach ambulatoryjnych, a 70%
pacjentów opuszczało ośrodek bez cewnika. Indeks nasilenia objawów zmniejszył się z 22 do 4 pkt., a wartość Qmax wzrosła z 9,4
do 20 ml/s.
Podsumowanie
TUNA i TUMT to proste i bezpieczne techniki, które u większości
chorych mogą być wykonywane w znieczuleniu miejscowym. Obie
te techniki pozwoliły na istotną poprawę wyników czynnościowych, jednak nie osiągnęły takiego samego poziomu skuteczności
i trwałości wyników jak TURP. Ich przewagą jest niższy odsetek powikłań oraz mniejsze wymagania dotyczące znieczulenia (ryc. 5).
Według wytycznych Europejskiego Towarzystwa Urologicznego
TUMT i TUNA powinny zostać zarezerwowane dla chorych, którzy
chcą uniknąć operacji lub nie reagują pozytywnie na leczenie
farmakologiczne. Podczas 6. Międzynarodowych Konsultacji nt.
Nowości w Leczeniu Raka Stercza i Chorób Stercza stwierdzono,
iż zabiegi TUNA i TUMT są opcjonalnymi metodami leczenia zabiegowego za wyjątkiem przypadków, gdy istnieją bezwzględne
wskazania do leczenia zabiegowego.
|
|
 |
HoLEP i KTP wykazują podobną skuteczność i wymagają podobnego znieczulenia jak TURP. Co więcej, ich skuteczność nie zależy od wielkości gruczołu krokowego, a profil bezpieczeństwa wydaje się być nieco lepszy niż dla TURP. HoLEP wiąże jest jednak z długą krzywą uczenia, dużym kosztem zakupu i trudnościami w usunięciu tkanki. KTP charakteryzuje się dłuższym czasem operacji, brakiem tkanki do oceny histopatologicznej oraz wysokim kosztem, m.in. spowodowanym jednorazowym użyciem włókien. Poza tym ciągle brakuje danych z długoterminowych badań nad KTP.
We wnioskach z 6. Międzynarodowych Konsultacji nt. Nowości
w Leczeniu Raka Stercza i Chorób Stercza stwierdzono, że HoLEP może być równoważny z TURP i adenomektomią, natomiast KTP wymaga dalszych badań.
Porównanie TUMT, TUNA, HoLEP i KTP z TURP oparto na podstawie wyników IPSS oraz Qmax (tab. 1). Średnie ważone różnic między poszczególnymi minimalnie inwazyjnymi metodami leczenia oparte zostały na podstawie wyników metaanaliz (oprócz KTP, które zostało oparte tylko na podstawie jednego randomizowanego badania kontrolnego).
Opracowała: Katarzyna Kocznur
SKN przy Katedrze i Klinice Urologii Ogólnej, Onkologicznej i Czynnościowej Warszawskiego Uniwersytetu Medycznego
